Kadmiyum, cd, atom numarası 48
Kadmiyum fiyatı, tarihçesi, oluşumu, çıkartılması ve kullanılması
Kadmiyum (ayrıca nadiren kadmiyum, Yunan kadαδμία kadmía, Latin cadmea, 'oksidik veya karbonat içeren çinko toprağı'), Cd elementi ve 48 atom numarasına sahip kimyasal bir elementtir. Genellikle geçiş metalleri arasında sayılır, ancak kapalı bir kabuğa sahiptir ve dolayısıyla ana grup elementlerine, özellikle de toprak alkali metallere benzer. Periyodik tabloda 5 içerisindedir. 2'in yanı sıra dönem. Alt grup (grup 12) veya çinko grubu.
Tarih
1817 bağımsız olarak Friedrich Stromeyer ve Carl Samuel Hermann tarafından kirlenmiş çinko karbonattaki kadmiyumu keşfetti. Stromeyer, kirlenmiş çinko karbonatın ısıtmada renksiz olduğunu fark etti - saf çinko karbonat göstermeyen bir davranış. Neredeyse 100 yıl boyunca, metal yalnızca Almanya'da kazanıldı.
Yaşlı Pliny, 77 doğa tarihi boyunca, Germania'daki Galmeifunden’in Naturalis tarihçisi: “cadmea […] almanya eyaleti repertumundaki ferman nuper etiam“ (Almanca: “geçenlerde Germania Galmei eyaletinde bulundu”). Kadmiyum terimi Orta Çağ'da, muhtemelen çinko ya da karbonat cevheri için kullanılmıştı. İmparator Frederick II tarafından Nisan 1226’ta Ravenna’da yayınlanan bir belgenin kanıtladığı gibi bu, Lavanttal’daki Benedictine Manastırı’nın Lavanttal’da bulunan St. Pauline Manastırı’nın "ad opus suum" (Almanca: "manastır alanında bulunan çinko ve gümüş ile kurşun ve demirin amacı için kullanılır").
Kadmiyum ve bileşiklerinin toksisitesine rağmen, 1907'in İngiliz Farmasötik Kodeksinin kadmiyum iyodürü, kese (skoröz bezler) ve chilblainler (skoröz bezler) için bir tedavi olarak kullandığı gösterilmiştir.
1907, Ångström'ü, 1 / 6438,4696, kuru havadaki kırmızı spektral kadmiyum çizgisinin dalga boyunun, 0,03 ° C'lik bir sıcaklıkta% 15 karbon dioksit içeriğine ve 1 atm basıncına çarpması olarak tanımlamıştır. 1960 Genel Ağırlıklar ve Ölçüler Konferansı, bir metrenin ikincil tanımı olarak kırmızı spektral kadmiyum çizgisinin 1.553.164,13 kat dalga boyunu kabul etti.
1942, dünyanın ilk nükleer reaktöründe Enrico Fermi kadmiyum levhaları kullandı. Zincirleme reaksiyonu kontrol etmek için tabakalar reaktörün içine ve dışına itilebilir. Kadmiyum ılımlı aralık nötronları yakalayabilir ve böylece reaktörün kritikliğini etkileyebilir.
Bulunduğu
Kadmiyum çok nadir bulunan bir elementtir. Yer kabuğundaki payı sadece 3 · 10 civarındadır-5 . Kadmiyum, doğal formunda, yani temel formunda oldukça nadirdir. Şimdiye kadar üç ülkede sadece beş bölge biliniyor: Vilyui Havzasındaki Khann'ya Nehri, Verkhoyansk yakınlarındaki Jana Nehri Havzası ve Rusya Sakha Cumhuriyeti’ne (Yakutya, Doğu Sibirya) Billeekh Saldırısı; Goldstrike çukurları, Nevada, Eureka County'deki Lynn yakınlarındaki ve Kazakistan'ın Aqumola bölgesindeki Burabaiskii masifi.
Kadmiyum içeren cevherler esas olarak,% 77,81 Cd'ye kadar GreenMackit (CdS) ve% 3 Cd'ye kadar bilinen Kadmiyum spat Otavit (CdCO65,20) ve ticari bozunma için çok nadir görülen kadmiyum ekranıdır. Her ikisi de neredeyse her zaman sfalerit (ZnS) ve smithsonit (ZnCO3) gibi çeşitli çinko cevherleriyle ilişkilidir.
Şimdiye kadar (2018 standında), 20 kadmiyum minerallerinden daha fazla bir şey bilinmektedir. Çok nadir kadmiyum oksit Monteponit,% 87,54'e kadar en yüksek Cd içeriğine sahiptir. Diğer mineraller arasında Hawleyit (% 77,81 Cd), Kadmoselit (% 58,74 Cd) ve Drobecit (IMA 2002-034,% 40,07% Cd) bulunur.
Mineral olarak kadmiyum
Doğal formda meydana gelen kadmiyum, temel formunda önce 1979 BV Oleinikov, AV Okrugin ve NV Leskova tarafından tarif edilmiştir. ve Uluslararası Mineraloji Derneği (IMA) tarafından bağımsız bir mineral türü olarak tanınmıştır (IMA Dahili Katılım Numarası: 1980-086a).
Strunz (9 baskısı) kadmiyuma göre minerallerin sınıflandırılmasına göre sistem no. 1.AB.05 (Elementler - Metaller ve Metaller - Çinko-Pirinç Ailesi - Çinko Grubu). Modası geçmiş 8 içinde. Bununla birlikte, kadmiyum Strunz'un Mineral Sistematiği baskısında henüz listelenmemiştir. Sadece 2018’in güncellendiğinde, özel koleksiyoncular ve kurumsal koleksiyonlar için dikkate alınan bu sistem biçimine dayanan “Lapis mineral rehberi” nde, sistem ve mineral no. I / A.4-40. Minerallerin ağırlıklı olarak İngilizce konuşulan ülkelerde kullanılan Dana'ya göre sınıflandırılması, sistemin altındaki mineral elementini no. 01.01.05.02.
Çıkarma ve sunum
Kadmiyum, yalnızca çinko eritme ve daha az oranda kurşun ve bakır eritme yan ürünü olarak elde edilir. Demir ve çeliğin geri dönüşümü için daha küçük miktarlar da geçerlidir.
Kadmiyum üretimi, çinkonun nasıl çıkarıldığına bağlıdır. Kuru çinko ekstraksiyonunda, kadmiyum ilk önce çinko ile azalır. Kadmiyum çinkodan daha düşük kaynama noktasına sahip olduğundan, daha kolay buharlaşır. Sonuç olarak, bir kadmiyum-çinko karışımı, indirgeme kabından buharlaşır ve başka bir yerde oksijen ile kadmiyum ve çinko okside reaksiyona girer. Daha sonra, bu karışım kok ile damıtma kabında karıştırılır ve kadmiyum çinkodan damıtılır. Kesirli damıtma, daha yüksek kadmiyum seviyelerine ulaşılmasını sağlar.
Islak çinko ekstraksiyonu sırasında, çözünmüş kadmiyum iyonları azaltılır ve çinko tozu ile çökeltilir. Elde edilen kadmiyum oksijen ile kadmiyum okside okside edilir ve sülfürik asit içinde çözülür. Elde edilen kadmiyum sülfat çözeltisinden, alüminyum anotlarla elektroliz ve kurşun katotlar, özellikle saf elektrolit kadmiyum elde edilir.
Fiziksel özellikleri
Kadmiyum, 8,65 g / cm3 yoğunluğunda gümüş renkli parlak bir metaldir. Yumuşaktır (Mohs sertliği 2), plastik olarak deforme edilebilir ve ayrıca telleri çekecek ve yaprakçıklara çekiç çekecek bir bıçakla kesilebilir.
Kadmiyum, yalnızca P63 / mmc uzay grubundaki altıgen kristal sisteminde katılaşır (alan grubu numarası 194). Saf kadmiyumun kafes parametreleri, birim hücre başına 0,2979 formül birimleri için a = 2,98 nm (0,5617 A'ya karşılık gelir) ve c = 5,62 nm'dir (2 A'ya karşılık gelir).
Teneke benzer şekilde, orta saflıktaki kadmiyum (teneke kalaylı kalay olarak adlandırılır) bükülürken tipik sesler ortaya çıkar. Cilalı kadmiyum birkaç gün sonra havadaki parlaklığını kaybeder, çinkoya göre korozyona daha dayanıklı olsa bile. Karbonatlı havada, grimsi beyaz, karbondioksit içeren bir kaplama oluşturur. Ağır bir şekilde ısıtıldığında, kırmızımsı ila sarı alev ile kahverengimsi kadmiyum oksit kadmiyum dioksit yakar.
CdO, II. Dünya Savaşı sırasında ABD tarafından kimyasal bir savaş ajanı olarak uygunluğu açısından yüksek toksisitesine karşı test edildi.
Kimyasal özellikleri
Kimyasal bileşiklerde genellikle iki değerlidir. Kimyasal olarak çinkoya benzer, ancak 4 koordinasyon numarasıyla karmaşık bileşikler oluşturma eğilimindedir. Havada kadmiyum oksidasyon nedeniyle yüzeyin kararmasına neden olur. Alkali ortamda, yüzey çözünmez, sülfürik asit ve hidroklorik asit bakımından ağır ve nitrik asit içinde kolayca çözünür.
Kullanım
Kadmiyumun yüksek toksisitesinden dolayı önemi azalır. Aralık 2011’tan bu yana Avrupa Birliği’nde mücevher, lehim ve PVC alaşımları yasaklandı. Kadmiyum kullanıldı veya kullanıldı:
- demir malzemelerinde korozyon koruması olarak (kadmiyum kaplama)
- askeri mühendislikte alüminyum malzemeler için yüzey kaplaması olarak (örneğin roketatarlar)
- nikel-kadmiyum piller için
- sarı ve koyu kırmızı renkte kadmiyum sülfit ve kadmiyum selenit pigmentleri boyalar ve plastikler için (bu arada, muhtemel sağlık tehlikeleri nedeniyle, özellikle ilgili maddeleri yakarken düşük pratik önem taşır)
- düşük erimeli alaşımlarda alaşım metalleri, örneğin rulman malzemeleri veya Wood metalleri
- Disk frenlerde yağlamadan daha erken
- Lehim malzemelerinin bir bileşeni olarak (lehim), ayrıca lehim alaşımları
- yarı iletken üretimi için
- Siyah beyaz televizyon tüplerinde fosfor olarak kadmiyum oksit ve mavi ve yeşil renkli tüplerde fosfor eklenmesi
- Anahtarlama kontaklarında gümüşe katkı olarak kadmiyum oksit
- Nötron yakalama için 113 izotopunun özellikle yüksek kesiti nedeniyle nükleer teknolojide termal nötronlara ve kontrol çubuklarına karşı koruyucu bir malzeme olarak
- Termal nötronlardan yüksek enerjili bir gama radyasyonu kaynağı (7 MeV civarında) olarak
- Spektral duyarlılığı insan gözüne benzer olan pozmetrelerde kadmiyum sülfit
- Kameralar için kızılötesi duyarlı bir sensör olarak kadmiyum tellürür (odak düzlemi dizileri)
- İnce film güneş pillerinde güç üretimi için kadmiyum tellürid veya kadmiyum sülfit olarak
- Cd, plastiklerde, örneğin PVC'de (ışığa duyarsız, ancak olası sağlık tehlikeleri nedeniyle düşük pratik öneme sahip olan) stabilize edici olarak stearat
- daha önce Weston Normal Elementleri'nde voltaj ölçü birimini belirlemek için 1 volt
- Sigortalar için kadmiyum bizmut alaşımları
- Gümüş-kadmiyum alaşımları, deoksidize olarak sterlin gümüş üretiminde
- takı için: altın yeşili altın kadmiyum alaşımları
- Kadmiyum lambası
- Helyum-kadmiyum lazerleri
- Elektrofizyolojide voltajla aktive olan kalsiyum kanallarını tıkayan kadmiyum iyonları
kadmiyum sülfit, selenit ve tellürit veya bunların karışımlarını ilave ederek sarı, turuncu ve kırmızı camları renklendirmek için.
Kadmiyum kalkojenitler kadmiyum sülfit (sarı), kadmiyum selenit (kırmızı) ve kadmiyum tellürid (siyah) önemli II-VI yarı iletkenleridir. Örneğin, kuantum noktaları (kuantum noktaları) olarak nanopartikülatlar üretilir ve diğerleri arasında, in vitro biyokimyada kullanılırlar.
kanıt
Kadmiyumun ön bir örneği olarak, Glühröhrchenprobe denilen hizmet verebilir. Bu amaçla, bazı stok maddeleri yüksek erime noktalı bir Glühröhrchen'de ısıtılır ve sonuçta ortaya çıkan sülfit-oksit karışımı, sodyum oksalat ile metallere indirgenir. Uçucu bir bileşen olarak, kadmiyum buharlaşır ve borunun üst kısmında metal bir ayna olarak biriktirir.
Daha sonra kükürt ve yenilenen tavlamanın ilave edilmesiyle, kadmiyum sülfit, metal ayna ve kükürt buharından oluşur; bu, oda sıcaklığında sıcağa kırmızı ve sarıdır. Bu renk değişimi birkaç kez tekrarlanabilir.
Kadmiyum katyonları için tespit reaksiyonu, sarı kadmiyum sülfit olarak sülfit çözeltisi veya hidrojen sülfit-su ile çökeltmedir. Diğer ağır metal iyonları bu algılamaya müdahale eder, böylece katyon ayrımı yapılmadan önce.
Kadmiyum izlerinin kantitatif tayini için polarografi önerilir. Kadmiyum (II) iyonları, -1 V'de (SCE'ye göre) 0,64 M KCl'de bir seviyeye girer. Ultra iz aralığında, cıva elektrotlarında ters voltametri kullanılabilir. Çok hassas, aynı zamanda kadmiyumun AAS grafit tüpüdür. Burada, 0,003 μg / l hala tespit edilebilir. Nispeten uçucu element yüksek bir piroliz sıcaklığına tolerans göstermez. Paladyum magnezyum nitrat gibi bir matris değiştirici yardımcı olabilir.
emniyet
Kadmiyum çok toksiktir ve bileşikleri zararlı (kadmiyum tellürit gibi), toksik (örn. Kadmiyum sülfit) veya çok toksik (kadmiyum oksit); ayrıca insanlarda kanserojen bir etkiye dair makul bir kuşku var. Alınan kadmiyum içeren toz akciğerlere, karaciğere ve böbreklere zarar verir.
Isıtılmış kadmiyum bileşiklerinin kullanıldığı çalışma alanlarında (lehimleme istasyonları ve kadmiyum banyoları), iyi havalandırma veya özütleme sağlar. Kimyasal Madde Bağımlılığı Yönetmeliğine göre, plastikteki kadmiyum içeriği ağırlıkça yüzde 0,01'i (100 mg / kg) geçmemelidir. Bu sınır Avrupa Birliği genelinde geçerlidir.
Aralık ayından bu yana 2011, plastiklerde, boyalarda, stabilizatörlerde ve REACH Yönetmeliği uyarınca bazı metal işlemlerinde kadmiyuma daha katı bir yasak uyguladıktan sonra, Ek XVII'deki 23'a girdi. Önceden, gümüş lehimleme tipik olarak% 10 ila% 25 kadmiyum,% 30'e kadar çocuk takı,% 0,2 PVC'dir. 10 ile. Aralık ayında 2011, kadmiyum içeren lehimlerin lehimleme yasağı ve kadmiyum kaplı mücevherlerin üretimi ve pazarlanması yasaklandı. Ek olarak, PVC geri dönüşümü hariç tüm PVC içeren ürünler de dahil edildi. 2016 Yönetmeliği (AB) 217 / 16. Şubat 2016’ta, REACH Tüzüğü Ek XVII’deki 23’e belirli boya ve verniklerdeki kadmiyum eklendi. Ek olarak, bazı boya ve cilalardaki kadmiyum içeriği, çinko içeren veya içerdiği ürünlerle sınırlandırılmıştır. Örneğin, kablosuz elektrikli cihazlarda Ni-Cd pillerin yüksek güç yoğunluğu nedeniyle istisnalar vardır.
toksikoloji
Kadmiyum, kimya endüstrisinde kaçınılmaz bir çinko, kurşun ve bakır özütleme ürünüdür. Kadmiyum ayrıca gübrelerde ve böcek ilaçlarında da bulunur.
Kayıt ve tehlikeler
Dünya Sağlık Örgütü, son yıllarda tolere edilebilir kadmiyum alımı ile ilgili açıklamasını, en son 2013 kilogramı başına kilogram başına 25 ag tolere edilebilir aylık alımına (TMI) düşürdü. Avrupa Gıda Güvenliği Otoritesi 2009’i her hafta vücut ağırlığının kilogramı başına kabul edilebilir düzeyde 2,5 μg seviyelerinde düşürdüğünü (TWI) vermiştir.
Kadmiyum insanlar tarafından çoğunlukla gıdalar tarafından emilir. Kadmiyum bakımından zengin yiyecekler şunlardır: karaciğer, mantar, kabuklu deniz ürünleri ve diğer kabuklu deniz ürünleri, kakao tozu ve kurutulmuş deniz yosunu. Ek olarak, keten tohumu çok miktarda kadmiyum içerir, bu nedenle günlük olarak 20 g'den fazla keten tohumu çekmemesi önerilir. Ayrıca, suni gübrelerin piyasaya sürülmesinden bu yana, tarım arazisinde ve dolayısıyla hemen hemen tüm gıdalarda kadmiyum birikimi olmuştur. Fosfatların kaynakları sınırlıdır ve çoğu kaynak kadmiyum veya radyoaktif ağır metallerle kirlenmiştir. Fosfat yataklarının kadmiyum içeriği çok farklıdır. Pek çok sanayileşmiş ülke gübrelerde kadmiyum sınırını çoktan attı. Avusturya'da kadmiyum konsantrasyonu, 75 mg / kg P2O5 ile sınırlıdır. Aynı zamanda, tütün dumanı, vücutta kanla yayıldığı yerden akciğerlere nispeten büyük miktarlarda kadmiyum taşır.
Özellikle yüksek kadmiyum fabrikalarında çalışan insanlar yüksek risk altındadır. Ancak vahşi çöplüklerden ve metal işlerinden kaynaklanan tehlikeler de var. Kadmiyumu solumak akciğerlere ciddi şekilde zarar verebilir ve hatta ölüme neden olabilir. Sanayideki kazalar - Çin'in Guangdong eyaletinde olduğu gibi - ve Itai Itai hastalığında (insanlarda) ve Gressenicher hastalarında (hayvanlarda otlatmada) olduğu gibi onlarca yıllık emisyonlar gerçek tehlikeleri açıkça ortaya koyuyor.
İnsanlarda hasar
Kadmiyum, endüstriyel veya çevresel nedenlerden dolayı vücutta kademeli olarak birikebilir ve tanınması zor bir kronik zehirlenmeye neden olabilir.
Kadmiyum, barsakta diyetten yaklaşık% 5 oranında emilir. Demir ve kalsiyum eksikliğinde, emme hızı artar, bu üç metalin hepsinin aynı taşıma yolunu kullandığını gösterir. Kadmiyum ilk önce karaciğerde, bir kompleksi oluşturduğu ve kan akımı yoluyla böbrek tübüllerinden geri döndürüldüğü ve renal glomerüllere taşındığı metalotiyoninlerin sentezini uyarır. Tübül hücrelerinde, metalotiyonin-kadmiyum kompleksi metabolize edilir ve Cd serbest bırakılır. Burada yine, cd daha fazla kadmiyumu bağlayan artmış metalthione sentezini aktive eder. Böbreklerde birikme, bu organa zarar vererek proteinüri ile sonuçlanır. Bu protein bağlanma kadmiyumundan dolayı sadece aşırı yavaş salınır, vücut için yarı ömür 30 yıl kadar kalır. Bu nedenle kadmiyum içeriği doğumdan itibaren artar ve 50-60 yıllarında tekrar düşer.
Kadmiyum aynı zamanda kemiklere de zarar verir, çünkü sonuçta kalsiyumun mobilizasyonuna neden olur. Cd, barsakta, barsak mukozasındaki Ca-bağlayıcı protein üzerindeki bağlanma bölgeleri için kalsiyum ile yarışır. Ek olarak, Cd, 1,25-dihidroksikolekalsiferolün (kalsitriol) böbrek tübül hücrelerinde yeniden sentezini engeller. 1,25-Dihidroksikolekalsiferol, intestinal mukoza hücresindeki kalsiyum bağlayıcı proteinin sentezini aktive etmek için gereklidir. Özetle, kadmiyum, bağırsak ve böbrekte kalsiyumun yeniden emiliminin azalmasına ve ayrıca, kemiklerden kalsiyum salınımının bir sonucu olarak idrarla artan atılım ve bunun da aynı şekilde bozulmasına neden olur.
Akut kadmiyum zehirlenmesi durumunda, biliyer atılım penisilinlamin veya dimerkaprol verilmesi ile desteklenebilir. Etkili, akut kadmiyum zehirlenmesinin tedavisinin ötesinde bilinmemektedir.
semptomlar
- İshal, karın ağrısı ve şiddetli kusma
- böbrek hasarı
- kemik kırıkları
- Merkezi sinir sistemine hasar
- Bağışıklık sistemine zarar
- Üreme bozuklukları ve hatta kısırlık
- Ruhsal bozukluklar
- Olası DNA hasarı ve karsinojenez
- Koku duyusunun kaybı
Bağlantıları
→ Kategori: Kadmiyum bileşiği
Oksitler ve hidroksit
- Kadmiyum oksit CdO
- Kadmiyum hidroksit Cd (OH) 2
halidler
- Kadmiyum florür CdF2
- Kadmiyum klorür CdCl2
- Kadmiyum bromür CdBr2
- Kadmiyum iyodür CdI2
kalkogenidler
- Kadmiyum sülfit CdS
- Kadmiyum selenid CdSe
- Kadmiyum tellürür CdTe
Diğer bileşikler
- Kadmiyum sülfat CdSO4
- Kadmiyum nitrat Cd (NO3) 2
- Kadmiyum siyanür Cd (CN) 2
- Kadmiyum Stearat Cd (C17H35COO) 2
Kadmiyum Fiyatı -> Stratejik Metal Fiyatları
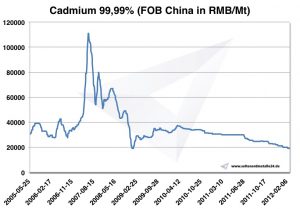
Grafik Kadmiyum 2005-2012


