İtriyum, Y, atom numarası 39
Genel Bilgileri
İtriyum [ʊtriʊm], Y sembol simgesi ve sıra numarası 39 olan kimyasal bir elementtir. Periyodik tablodaki 5'teki geçiş metallerine ve nadir toprak metallerine aittir. 3'in yanı sıra dönem. Alt grup (grup 3) veya skandiyum grubu. Yttrium, ilk bölgeden, Stockholm yakınlarındaki Ytterby madeninin yanı sıra Ytterbium, Terbium ve Erbium olarak adlandırılmıştır.
Yttrium (Ytterby'den, İsveç'in başkenti Stockholm yakınındaki bir maden) Maden Ytterbit'teki Johan Gadolin 1794 tarafından keşfedildi. 1824, Friedrich Wöhler 'in potasyum ile itriyum klorürü indirgeyerek itriyumla kirlenmiş üretti. Sadece 1842, Carl Gustav Mosander'ı, itriyumu eşlik eden elementlerden erbiyum ve terbiyumdan ayırarak başardı.
İtriyum, temel durumda doğada bulunmaz. İtriyum içeren mineraller (Yttererden) daima diğer nadir toprak metalleriyle ilişkilendirilir. Uranyum cevherlerinde de bulunabilir. % 3 itriyumlu monazit kumları ve% 0,2 itriyumlu bastnasit ticari olarak parçalanabilir. Ayrıca, xenotime'nin ana bileşenidir (Y [PO4]).
Büyük Monazitvorkommen, 19'in başlangıcı. 20. yüzyılda Brezilya ve Hindistan'da keşfedilen ve sömürülen bu iki ülke, büyük itriyum cevheri üreticileri haline geldi. Sadece 1990'lere kadar büyük miktarlarda bastnasit üreten Kaliforniya'daki Mountain Pass Mine'ın açılması, ABD'yi az miktarda itriyum içermesine rağmen, asfaltın asıl üreticisi haline getirdi. Bu madenin kapanmasından bu yana, Çin, 60% 'in en az bulunan nadir toprak üreticisidir. Bunlar, cevheri ksenotime içeren Bayan Kuang yakınlarındaki bir madende ve daha çok Çin'in güneyinde mayınlı olan iyon emici kil minerallerinden elde edilmektedir.

İtriyum metal
kurtarma
Nadir toprakların birbirinden ayrılması, itriyum üretiminde zahmetli bir adımdır. Serum çözeltilerinin fraksiyonel kristallenmesi, başlangıçta, nadir toprakların laboratuvar ölçeğinde ayrılmasında kullanılan ilk yöntemdi. Sadece iyon kromatografisinin eklenmesi, nadir toprakları endüstriyel ölçekte ayırmayı mümkün kılmıştır.
Konsantre itriyum oksit, floride dönüştürülür. Metale daha sonra indirgeme, vakumlu endüksiyon ocağındaki kalsiyum ile meydana gelir.
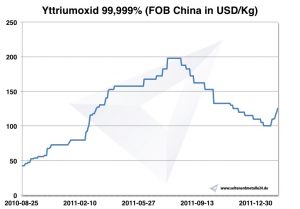
Grafik itriyum oksit 2010-2011
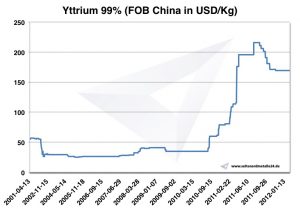
Grafik Yttrium 2001-2012
Özellikler
İtriyum havada nispeten kararlıdır fakat ışık altında kararır. 400 ° C'nin üzerindeki sıcaklıklarda, taze arayüzler tutuşabilir. İnce bölünmüş itriyum nispeten kararsızdır. İtriyum, nötronlar için düşük bir yakalama kesitine sahiptir.
Bileşiklerinde çoğunlukla üç değerliklidir. Bununla birlikte, itriyumun <3 oksidasyon durumlarını alabildiği küme bileşikleri de vardır.
32Y ve 76Y arasında ve ayrıca bilinen diğer 108 çekirdek izomerleri arasında toplam 24 izotopları vardır. Bunlardan yalnızca doğal itriyumun var olduğu sadece bir 89Y sabittir. İtriyum, 22 saf elementlerinden biridir. En stabil radyoizotoplar, yarı ömrü 88 gün olan 106,65Y ve yarı ömrü 91 gün olan 58,51Y'dir. Diğer tüm izotoplar, yarı ömrü 87 saat olan 79,8Y ve 90 saat olan 64Y hariç, bir günün altında yarı ömre sahiptir. İtriyum izotopları, nükleer reaktörlerde ve nükleer patlamalarda uranyum fisyonunun en yaygın ürünleri arasındadır.
Periyodik Tablo itriyum-39
Kullanım
Tüp reaktör teknolojisinde metalik itriyum kullanılır. Bir itriyum-kobalt alaşımı kalıcı bir mıknatıs olarak kullanılabilir. İtriyum, kütle spektrometrelerinin iyon kaynaklarındaki telleri ısıtmak için bir malzeme olarak kullanılır. Metalurjide, küçük demir itriyum katkı maddeleri, örneğin demir-krom-alüminyum ısı iletken alaşımlarında, krom, molibden, titanyum ve zirkonyum alaşımlarında tahıl rafine etmek için kullanılır. Alüminyum ve magnezyum alaşımlarında güçlendirici bir etkiye sahiptir. Teknik olarak daha önemli olan oksidit itriyum bileşikleridir:
Manto içinde kaplama malzemesi olarak itriyum nitrat
Yttrium alüminyum granat (YAG), bir lazer kristali olarak işlev görür
Mikrodalga filtresi olarak Yttrium demir garnet (YIG)
Yakıt hücrelerinde katı elektrolit olarak itriyum stabilize zirkonya (SOFC, Katı Oksit Yakıt Pili)
Bununla birlikte, itriyum oksitlerin ve itriyum oksit sülfürlerin en önemli kullanımları, televizyon resim tüplerinde, flüoresan lambalarda ve radar tüplerinde üç değerlikli europium (kırmızı) ve thulyum (mavi) katkılı fosforlarda (fosforlar) çok yönlülüktür.
Ayrıca, itriyum seramik ve alaşımları da kullanılır:
Lambda sondalar
Süper iletkenler (örneğin, itriyum-baryum-bakır oksit YBa2Cu3O7-x)
ODS alaşımlar
kıvılcım
Saf bir beta yayıcı olarak, 90Yttrium, nükleer tıpta, örneğin Radiosynoviorthese gibi terapi için kullanılır.
İtriyum, gereksiz ve toksik olarak kabul edilir (MAK değeri = 5 mg / m3).
| Allgemein | ||
| İsim, sembol
sıra |
İtriyum, Y, 39 | |
| dizi | Geçiş metalleri | |
| Grup, dönem, blok | 3, 5, d | |
| Görünüş | gümüşi beyaz | |
| CAS numarası | 7440-65-5 | |
| Dünya zarfının kütle oranı | 26 ppm | |
| nükleer | ||
| atomik kütle | 88,90585 u | |
| atomik yarıçap | 180 pm | |
| Kovalent yarıçapı | 190 pm | |
| Elektronenkonf. | [Kr] 4d (1) 5s2 | |
| 1. iyonlaşma | 600 KJ / mol | |
| 2. iyonlaşma | 1180 KJ / mol | |
| 3. iyonlaşma | 1980 KJ / mol | |
| fiziksel olarak | ||
| Fiziksel durum | fest | |
| kristal yapı | altıgen şeklinde | |
| yoğunluk | 4,472 g / cm3 | |
| manyetizma | paramanyetik (χm = 1,2 * 10 (-4)) | |
| ergime noktası | 1799 K (1526 C) | |
| kaynama noktası | 3609 K (3336 C) | |
| Molar hacmi | 19,88 * 10 (-6) m (3) / mol | |
| buharlaşma ısısı | 380 KJ / mol | |
| kaynaşma ısısı | 11,4 KJ / mol | |
| Elektriksel iletkenlik | 1,66 * 10 (6) A / (V * m) | |
| ısı iletkenliği | 17 W / (m * K) | |
