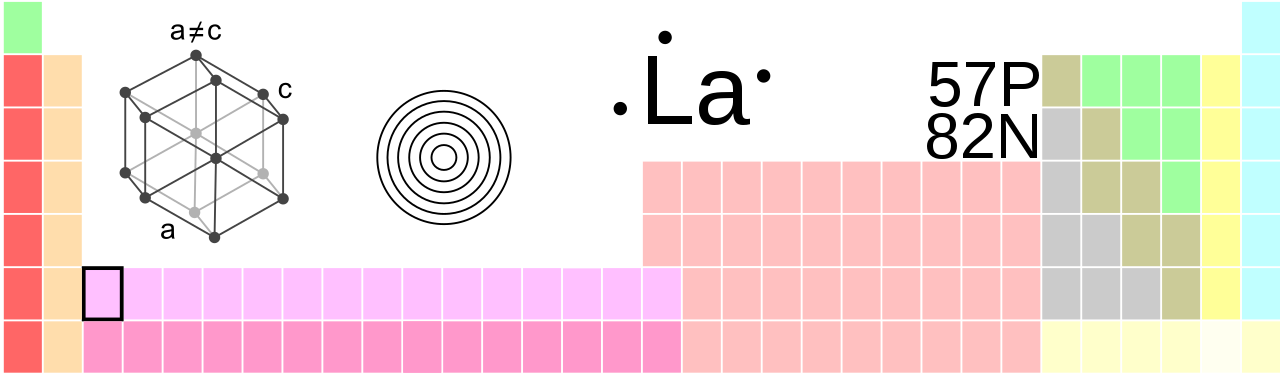
Lantan, La, atom numarası 57
Genel Bilgileri
Lantan [lantaːn], La element sembolü ve 57 atom numarasına sahip kimyasal bir elementtir. Nadir toprak metallerinin yanı sıra geçiş metallerine aittir, periyodik tablodaki 6 içinde durmaktadır. Dönem ve 3. Alt grup (grup 3) veya skandiyum grubu. Çoğunlukla, elementin f kabuğu boş olmasa bile, Lantaniden sayılır.
Lanthanum (Yunanca λανθάνειν, latanhane, "gizlenecek") 1839, İsveçli kimyacı ve cerrah Carl Gustav Mosander tarafından keşfedildi. Sözde saf seryum nitrattan fraksiyonel kristallenme Lantan sülfat ile kazandı.
Lantan doğal olarak sadece çeşitli minerallerdeki diğer lantanlarla bağlantılı kimyasal bileşiklerde bulunur. Temelde bunlar:
Monazit ((Ce, La, Th, Nd, Y) PO4)
Bastnäsit ((Ce, La, Y) CO3F)
kurtarma
Diğer latantan yoldaşının karmaşık bir ayrılmasından sonra, oksit, lantan florüre kadar hidrojen florür ile reaksiyona sokulur. Daha sonra, bu, kalsiyum florür oluşturmak üzere, kalsiyum ile lantanuma indirgenir. Kalan kalsiyum tortularının ve safsızlıkların ayrılması, vakum içinde ilave bir yeniden eritme işleminde gerçekleşir.
Özellikler
Simli beyaz metal dövülebilir ve yumuşaktır. Üç metalik değişiklik var.
Lantan tanımlanmamış. Havadaki beyaz bir oksit tabakası ile hızlı bir şekilde kaplanır ve nemli havada hidroksitle reaksiyona girer.
440 ° C üzerindeki sıcaklıklarda lantan, lantan okside (La2O3) yanar. Soğuk suda hidrojen oluşumu yavaştır, ılık suda hidroksite hızlı reaksiyon verir Seyreltik asitlerde lantan, hidrojenin evrimi altında çözünür, birçok element ile doğrudan ısıda, oda sıcaklığında bile halojenlerle reaksiyona girer. Lantan ve hidrojen siyah, suya duyarlı bir nontoichiometrik hidrid oluşturur.
Kullanım
Lantan, misch metalde bir bileşendir. Piroforik çakmaktaşı malzemeleri, 25 ila 45 ağırlık yüzdesi lantan içerir. Ek olarak, metalurjide indirgeyici bir ajan olarak kullanıldığını bulur. Dökme demir ilavesi olarak sferoidal grafit oluşumunu destekler, alaşım katkı maddesi olarak oksidasyon direncini arttırır. Lantan katkıları molibden sertliğini ve sıcaklık hassasiyetini azaltır.
Serbest elektronların üretilmesi için yüksek kaliteli katotlar, tungsten telinin yerine geçen lantan heksaboritten oluşur. Yüksek saflıkta lantan oksit, cam endüstrisinde, optik z için yüksek kırılma indisine sahip yüksek kaliteli camların üretiminde kullanılır. B. kamera lensleri için kullanılır.
Kobalt ile:
Kobalt-lantan alaşımlı LaCo5, PTC termistörlerin (sıcaklığa bağlı dirençler) üretimi için manyetik bir malzeme, lantan katkılı baryum titanat olarak kullanılır. Kobalt, demir, manganez, stronsiyum ve diğerleri ile birlikte, yüksek sıcaklıktaki yakıt hücreleri (SOFC) için bir katot görevi görür. "Kirlenmiş" lantan nikeli (LaNi5), nikel metal hidrit depo bataryalarında hidrojen depolaması olarak kullanılır. Ayrıca stüdyo aydınlatması için karbon ark lambalarında ve Önceden film projeksiyon sistemlerinde (tarihsel uygulama?) Gelir.
Titanyum ile:
Lantan ve titanyumdan oluşan malzeme bileşimlerine sahip bir alaşım metal, etki, talaş oluşturma işleminde talaş uzunluğunun azaltılması gerçeğine bağlanır. Bu, metalin işlenmesini kolaylaştırmalıdır.
Tıp alanında, alaşım metalden korozyona dayanıklı ve kolayca sterilize edilebilir aletler üretilir. Bu titanyum bazlı metal alaşımının cerrahi aletler ve aparatlar için özellikle uygun olduğu söylenir, çünkü diğer metal alaşımlara göre titanyum ile bu tür metal alaşımlarını kullanmanın alerji eğilimi düşük olmalıdır.
Lantan oksit olarak
Kameralar, teleskop lensleri ve gözlük camları için, sırasıyla dalga boyunda (düşük dağılım) sadece biraz değişen, nispeten yüksek kırılma indisine sahip gözlük üretimi (Lanthanglas)
Kristal cam ve porselen lekelerinin üretimi. Aynı zamanda kimyasal direncin iyileştirilmesiyle (alkali direncinin iyileştirilmesi, "bulaşık makinesinde yıkanabilir") daha fazla toksik kurşun bileşiğinin yerini alır.
Petrol rafinerisinde akışkanın katalitik çatlaması sırasında zeolitlere katalizör eklenmesi
Seramik kondansatör kütlelerinin ve silikatsız camların üretimi
Cam parlatıcıların bileşeni
Elektron tüpleri için sıcak katot üretimi (ayrıca lantan boridleri)
Lantan karbonat olarak
Diyaliz hastalarında fosfat seviyesinin düşürülmesi için ilaç (sözde fosfat bağlayıcı)
Lantan, toksisite düşük olarak sınıflandırılır. Toksik bir doz bilinmemektedir. Bununla birlikte, lantan tozu çok aşındırıcı olarak kabul edilir, çünkü örneğin cilt nemi ile bazik lantan hidroksitine (kalsiyum ve stronsiyum elementlerine benzer) çok kolay tepki verir. Sıçanlarda öldürücü doz 720 mg'dır.
| Allgemein | |
| İsim, sembolSipariş numarası | Lantan, La, 57 |
| dizi | Geçiş metalleri |
| Grup, dönem, blok | 3, 6, d |
| Görünüş | gümüşi beyaz |
| CAS numarası | 7439-91-0 |
| Dünya zarfının kütle oranı | 17 ppm |
| nükleer | |
| atomik kütle | 138,9055 u |
| atomik yarıçap | 195 pm |
| Kovalent yarıçapı | 207 pm |
| Elektronenkonf. | [Xe] 5d (1) 6s2 |
| 1. iyonlaşma | 538,1 KJ / mol |
| 2. iyonlaşma | 1067 KJ / mol |
| 3. iyonlaşma | 1850 KJ / mol |
| fiziksel olarak | |
| Fiziksel durum | fest |
| kristal yapı | altıgen şeklinde |
| yoğunluk | 6,17 g / cm3 (20 ° C) |
| manyetizma | paramanyetik (χm = 5,4 * 10 (-5)) |
| ergime noktası | 1193 K (920 C) |
| kaynama noktası | 3743 K (3470 C) |
| Molar hacmi | 22,39 * 10 (-6) m (3) / mol |
| buharlaşma ısısı | 400 KJ / mol |
| kaynaşma ısısı | 6,2 KJ / mol |
| Elektriksel iletkenlik | 1,626 * 10 (6) A / (V * m) |
| ısı iletkenliği | 13 W / (m * K) |
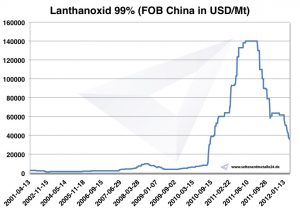
Lantan fiyatı